BCAA jako lek?

Skutki niedoboru i nadmiernego spożycia BCAA
Jak wspomniałam wcześniej, niedobory w spożyciu aminokwasów rozgałęzionych występują niezwykle rzadko. Powodem takiego stanu rzeczy może być dieta ale też choroby nerek oraz wątroby, które znacznie zaburzają metabolizm białek. Jak organizm manifestuje niedobrór BCAA? Najczęściej obserwuje się zmęczenie, depresje, drażliwość oraz zawroty i bóle głowy. Natomiast chronicznie i długotrwałe niedobory aminokwasów rozgałęzionych w diecie mogą prowadzić do znacznie poważniejszych nieprawidłowości - katabolizmu białek mięśniowych, zatrzymania wzrostu oraz zahamowania odbudowy tkanek [2]. Sprawnie funkcjonujący organizm bez trudu jest w stanie poradzić sobie nawet z wysokimi dawkami aminokwasów rozgałęzionych. Wszystko za sprawą dość sporego zapasu w aktywności enzymów biorących udział w metabolizmie BCAA w tkankach całego ciała. Oczywiste jest, że tak jak w przypadku każdej substancji dostarczanej do organizmu, muszą istnieć pewne granice w jej podaży, po przekroczeniu których ich metabolizm staje się niemożliwy – stoicyzm przede wszystkim!. W przypadku BCAA jednak, nie natrafiłam jeszcze na badania, które rzetelnie oceniłyby ich nadmiar w organizmie oraz spowodowane nim skutki uboczne.

Udział BCAA w przebiegu i profilaktyce niektórych chorób
- Fenyloketonuria
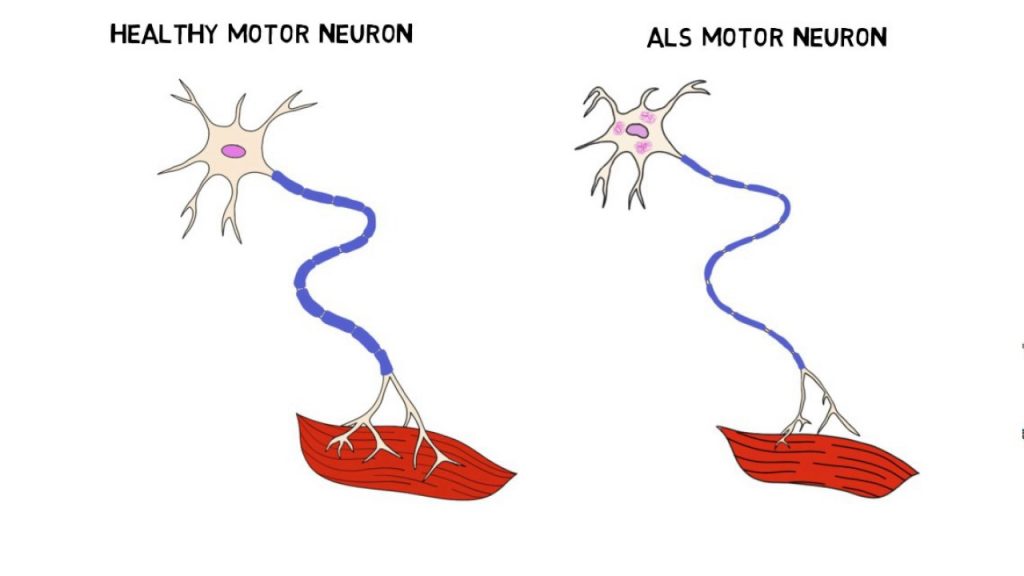 kwas glutaminowy jest neuroprzekaźnikiem pobudzającym, jego nadmierna ilość powoduje zbyt silną stymulację neuronów, co w konsekwencji prowadzi do ich śmierci. Jak BCAA może tutaj pomóc? W przypadku tej choroby, badano wpływ aminokwasów rozgałęzionych na wzrost aktywności dehydrogenazy GLU, zwiększenie tempa usuwania kwasu glutaminowego z mózgu, a w konsekwencji - na obniżenie neurotoksycznego efektu nadmiaru neuroprzekaźnika w płynach zewnątrzkomórkowych. Wyniki badań były zaskakujące. Wykazano, że roczna suplementacja dawką 26,4 g BCAA dziennie pacjentowi choremu na stwardnienie zanikowe boczne znacznie obniża tempo postępowania zmian neurologicznych w porównaniu z próbą kontrolną, nie powodując przy tym żadnych efektów ubocznych [9]. Niestety muszę dodać, że heterogenność i zmienność reakcji organizmu człowieka na leczenie jest jak zawsze czynnikiem determinującym skuteczność terapii. Inne badania wykazały bowiem uboczne efekty suplementacji takie jak wzrastająca śmiertelność i przyspieszone powstawanie niewydolności oddechowej. Jak dotąd nie ustalono jednoznacznego poglądu dotyczącego wpływu suplementacji BCAA na zmniejszanie objawów stwardnienia zanikowego bocznego.
5.Choroby wątroby: marskość, encefalopatia, rak wątroby
Wspólnym mianownikiem chorób wątroby jest nieprawidłowy metabolizm aminokwasów przejawiający się m. in. niskim poziomem krążących we krwi aminokwasów rozgałęzionych, a podwyższonym aminokwasów aromatycznych (fenyloalaniny, tryptofanu i tyrozyny) oraz metioniny. Dziś wiadomo już, że zwiększona podaż aminokwasów aromatycznych do mózgu wzmacnia produkcję neurotransmiterów oraz amin biogennych. Związki te uważane są za czynnik powstawania niebezpiecznych powikłań marskości wątroby, a w szczególności encefalopatii wątrobowej.
Najbardziej charakterystycznym objawem marskości wątroby jest postępujące włóknienie jej miąższu, co w konsekwencji prowadzi do niszczenia struktury tego narządu i całkowitego upośledzenia funkcji metabolicznych. Chorzy charakteryzują się podwyższonym tempem metabolizmu, przez co ich zapotrzebowanie na białko i aminokwasy jest również zwiększone. Jak wspomniałam na początku artykułu, metabolizm aminokwasów rozgałęzionych odbywa się w głównej mierze w mięśniach szkieletowych, podczas gdy pozostałe aminokwasy są metabolizowane przede wszystkim w wątrobie. I tu swoje miejsce znajduje wykorzystanie BCAA ! Udowodniono, że podczas gdy upośledzeniu uległy metaboliczne funkcje wątroby, suplementacja BCAA wywierała korzystny wpływ na utrzymanie bilansu azotu, a także nie prowadziła do encefalopatii wątrobowej, tak jak ma to miejsce w przypadku zwiększenia podaży azotu pochodzącego z większości białek pożywienia. Aminokwasy rozgałęzione, a w głównej mierze leucyna, aktywują ponadto syntezę czynnika wzrostu hepatocytów (HGF) – cytokiny, która bierze udział w regeneracji wątroby, a dodatkowo jest silnym miogenem (frakcja rozpuszczalnych w wodzie białek z komórek mięśniowych, które nie wchodząca w skład struktur filamentowych mięśnia). Suplementacja BCAA podczas marskości wątroby wydaje się być zatem zasadna, gdyż postępujące niszczenie hepatocytów może być częściowo hamowane przez zwiększenie tempa procesów odbudowy [10].
Korzystne działanie BCAA opisano także w kontekście hamowania rozwoju choroby nowtoworowej. Opublikowane w 2017 roku badanie obejmujące ponad 300 uczestników wykazało korzystny wpływ BCAA na hamowanie progresji nowotworu wątroby i lepsze rokowanie pacjentów [11].
Myślę, że przytoczone przeze mnie fakty wyraźnie wskazują, że warto spojrzeć na to „trio aminokwasów“ już nie tylko jako na element wspomagający trening (bądź, jak może się okazać w dalszej przyszłości, przeceniany w tym względzie suplement [12]...) ale bardzo istotny „terapeutyk“ w ciężkich nieprawidłowościach organizmu.
PS. Ja ochoczo jem i będę jadła BCAA bez względu na to czy działa w kontekście sportowym czy też nie ! :)
Źródła:
kwas glutaminowy jest neuroprzekaźnikiem pobudzającym, jego nadmierna ilość powoduje zbyt silną stymulację neuronów, co w konsekwencji prowadzi do ich śmierci. Jak BCAA może tutaj pomóc? W przypadku tej choroby, badano wpływ aminokwasów rozgałęzionych na wzrost aktywności dehydrogenazy GLU, zwiększenie tempa usuwania kwasu glutaminowego z mózgu, a w konsekwencji - na obniżenie neurotoksycznego efektu nadmiaru neuroprzekaźnika w płynach zewnątrzkomórkowych. Wyniki badań były zaskakujące. Wykazano, że roczna suplementacja dawką 26,4 g BCAA dziennie pacjentowi choremu na stwardnienie zanikowe boczne znacznie obniża tempo postępowania zmian neurologicznych w porównaniu z próbą kontrolną, nie powodując przy tym żadnych efektów ubocznych [9]. Niestety muszę dodać, że heterogenność i zmienność reakcji organizmu człowieka na leczenie jest jak zawsze czynnikiem determinującym skuteczność terapii. Inne badania wykazały bowiem uboczne efekty suplementacji takie jak wzrastająca śmiertelność i przyspieszone powstawanie niewydolności oddechowej. Jak dotąd nie ustalono jednoznacznego poglądu dotyczącego wpływu suplementacji BCAA na zmniejszanie objawów stwardnienia zanikowego bocznego.
5.Choroby wątroby: marskość, encefalopatia, rak wątroby
Wspólnym mianownikiem chorób wątroby jest nieprawidłowy metabolizm aminokwasów przejawiający się m. in. niskim poziomem krążących we krwi aminokwasów rozgałęzionych, a podwyższonym aminokwasów aromatycznych (fenyloalaniny, tryptofanu i tyrozyny) oraz metioniny. Dziś wiadomo już, że zwiększona podaż aminokwasów aromatycznych do mózgu wzmacnia produkcję neurotransmiterów oraz amin biogennych. Związki te uważane są za czynnik powstawania niebezpiecznych powikłań marskości wątroby, a w szczególności encefalopatii wątrobowej.
Najbardziej charakterystycznym objawem marskości wątroby jest postępujące włóknienie jej miąższu, co w konsekwencji prowadzi do niszczenia struktury tego narządu i całkowitego upośledzenia funkcji metabolicznych. Chorzy charakteryzują się podwyższonym tempem metabolizmu, przez co ich zapotrzebowanie na białko i aminokwasy jest również zwiększone. Jak wspomniałam na początku artykułu, metabolizm aminokwasów rozgałęzionych odbywa się w głównej mierze w mięśniach szkieletowych, podczas gdy pozostałe aminokwasy są metabolizowane przede wszystkim w wątrobie. I tu swoje miejsce znajduje wykorzystanie BCAA ! Udowodniono, że podczas gdy upośledzeniu uległy metaboliczne funkcje wątroby, suplementacja BCAA wywierała korzystny wpływ na utrzymanie bilansu azotu, a także nie prowadziła do encefalopatii wątrobowej, tak jak ma to miejsce w przypadku zwiększenia podaży azotu pochodzącego z większości białek pożywienia. Aminokwasy rozgałęzione, a w głównej mierze leucyna, aktywują ponadto syntezę czynnika wzrostu hepatocytów (HGF) – cytokiny, która bierze udział w regeneracji wątroby, a dodatkowo jest silnym miogenem (frakcja rozpuszczalnych w wodzie białek z komórek mięśniowych, które nie wchodząca w skład struktur filamentowych mięśnia). Suplementacja BCAA podczas marskości wątroby wydaje się być zatem zasadna, gdyż postępujące niszczenie hepatocytów może być częściowo hamowane przez zwiększenie tempa procesów odbudowy [10].
Korzystne działanie BCAA opisano także w kontekście hamowania rozwoju choroby nowtoworowej. Opublikowane w 2017 roku badanie obejmujące ponad 300 uczestników wykazało korzystny wpływ BCAA na hamowanie progresji nowotworu wątroby i lepsze rokowanie pacjentów [11].
Myślę, że przytoczone przeze mnie fakty wyraźnie wskazują, że warto spojrzeć na to „trio aminokwasów“ już nie tylko jako na element wspomagający trening (bądź, jak może się okazać w dalszej przyszłości, przeceniany w tym względzie suplement [12]...) ale bardzo istotny „terapeutyk“ w ciężkich nieprawidłowościach organizmu.
PS. Ja ochoczo jem i będę jadła BCAA bez względu na to czy działa w kontekście sportowym czy też nie ! :)
Źródła:
- Riazi R, Wykes LJ, Ball RO, Pencharz PB. The total branched-chaina mino acid requirement in young healthy adult men determined by indicator amino acid oxidation by use of L-[1–13C]phenylalanine. JNutr. 2003; 133: 1383–1389.
- Harris RA, Joshi M, Jeoung NH, Obayashi M. Overview of the molecular and biochemical basis of branched-chain amino acid catabolism. J Nutr. 2005; 135: 1527–153
- Makarewicz-Wujec M, Kozłowska-Wojciechowska M. Dieta w fenyloketonurii.2000.
- Pietz J, Kreis R, Rupp A, Mayatepek E, Rating D, Boesch Ch, i wsp. Large neutral amino acids block phenylalanine transport into brain tissue in patients with phenylketonuria. J Clin Invest. 1999; 103: 1169–1178.
- Richardson MA, Bevans ML, Read LL, Clelland JD, Suckow RF, MaherTJ, i wsp. Efficacy of the branched-chain amino acids in the treatmentof tardive dyskinesia in men. Am J Psychiat. 2003; 160: 1117–1124.
- Montgomery AJ, McTavish SF, Cowen PJ, Grasby PM. Reduction of brain dopamine concentration with diet ary tyrosine plus phenylalanine depletion: an [11c]raclopride PET study. Am J Psychiat. 2003;160: 1887–1889.
- Gijsman HJ, Scarna A, Harmer CJ, McTavish SB, Odontiadis J, Cowen PJ, i wsp. A dose-finding study on the effects of branch chain amino AIDS on sur rogate markers of brain dopamine function. Psychopharmacology. 2002; 160: 192–197
- Adamek D, Tomik B. Stwardnienie boczne zanikowe. ZOZ Ośrodek UMEA Shinoda-Kuracejo, Wyd. I Kraków, 2005
- Plaitakis A. Altered glutamate metabolism in amyotrophic lateral sclerosis and treatment with branched chain amino acids. Amino Acids pp 379-385
- Marchesini G, Marzocchi R, Noia M, Bianchi G. branched-chain amino acid supplementation in patients with liver diseases. J Nutr. 2005; 135: 1596–1601.
- Wolfie R.: Branched-chain amino acids and muscle protein synthesis in humans: myth or reality? ISSN 2017,14;30.
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5478300/
 ⮜ Poprzedni artykuł
⮜ Poprzedni artykuł
Waskularyzacja - jak poprawić definicję mięśni?
 Następny artykuł ⮞
Następny artykuł ⮞


